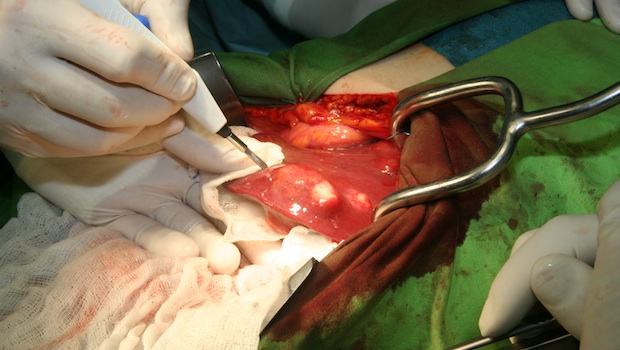
 Munkában az intelligens onko-kés. Forrás: Semmelweis Médiasarok
Munkában az intelligens onko-kés. Forrás: Semmelweis MédiasarokDr. Takáts Zoltán, a Semmelweis Egyetem (SE) kutatója által kifejlesztett eszköz lényegesen felgyorsítja a biológiai szövetek analízisét, csökkenti a ráksebészeti vizsgálat időtartamát, ugyanakkor megnöveli annak pontosságát, azaz képessé teszi az orvost arra, hogy gyorsabban és jobban döntsön a gyógyszer kiválasztásáról és adagolásáról. Az eszköz fő alkalmazási területe a ráksebészet, az érsebészet, illetve a bőrgyógyászati és a plasztikai sebészet. A feltaláló által írt ismertetőt közöljük.
Hírek a rákbetegség kezeléséről:
Új immunterápiás gyógyszerek - a bispecifikus antitestek
Első humán kísérlet a CRISPR-szerkesztett T-sejtekkel a rák személyre szabott kezelésére
Hormonterápia prosztatarák esetében
Nyelési problémák daganatos betegeknél
Célzott terápiákkal egyre hatékonyabban kezelhető a rák
Háttéranyagaink:
A rákbetegség kezelése összeállítás kezdőoldala
Sebészi kezelés
Kemoterápia
Sugárkezelés (sugárterápia, radioterápia)
Célzott daganatterápia
Őssejtterápia
Természetgyógyászat
Támogató (szupportív) kezelés
Háttér
Sebészeti beavatkozások során igen komoly problémát jelent a műtéti területen feltárt szövetrészletek hisztológiai szintű azonosítása, különösen rosszindulatú tumoros elváltozások műtéti terápiája esetében. A tumoros szövet gyakran nem különül el egyértelműen a környező egészséges szövettől, így pusztán vizuális információra támaszkodva a tumor nem távolítható el kellő biztonsággal. Ezen probléma megoldására számos technika született, azonban ezen technológiák egyike sem ad megnyugtató eredményt. A ma használatos megoldások felölelik a műtét előtti (esetleg közbeni) képalkotó vizsgálatokat, valamint a műtét során eltávolított tumor hisztológiai vizsgálatát. Ezen vizsgálatok közös problémája, hogy az eredmény nem kötődik közvetlenül a műtéti területen feltárt szövetrészletekhez, így csak közvetett információt hordoz magában.
A kutatás története
Kutatásunk legfontosabb célkitűzése egy olyan módszer kidolgozása volt, amelynek segítségével a szövetek azonosítása a műtéti területen elvégezhető és azonnali eredményt szolgáltat. A kutatás alapvető eszközéül a tömegspektrometria nevű analitikai kémiai technikát választottuk. A tömegspektrometriás módszerek a vizsgált mintákat alkotó molekulák tömegének a meghatározásán alapulnak. Kutatásunk kezdeti fázisában olyan tömegspektrometriás technikát képzeltünk el, amely képes biológiai szövetek közvetlen elemzésére. Mivel az élő szövetek sok százezer különféle molekulából állnak, az ilyen módon nyert információ egyrészt betekintést nyújthat az élő szervezet biokémiai folyamataiba, másrészt pedig lehetőséget teremthet a szövet egyedi sajátosságainak a feltérképezésére. A kutatási folyamat egyik legkockázatosabb lépése egy olyan ún. ionizációs technika kifejlesztése volt, amelyik egyrészt nem hordoz semmilyen veszélyt a betegre nézve, másrészt viszont képes az élő szövet molekuláit tömegspektrometriásan vizsgálható, elektromosan töltött részecskékké, azaz ionokká alakítani. Ezen feladat megoldása során a véletlen sietett segítségünkre, ugyanis felfedeztük, hogy a sebészetben általánosan használt elektrosebészeti eszközök a normális sebészeti beavatkozás során ionizálják a szövet egyes komponenseit, tehát a szokásos sebészeti eszköz minimális változtatásokkal használható a fent körvonalazott cél eléréséhez. Az elektrosebészeti eszköz ezt követően sikeresen kapcsoltuk a tömegspektrometriás műszerrel. Az ily módon létrejövő eszköz tulajdonképpen egy intelligens sebészeti eszköz, amely a vágáson (ill. koaguláláson) kívül képes tömegspektrometriás információt adni a szövetek molekuláris összetételéről. Mivel a nyers tömegspektrometriás információ a sebész felhasználók számára közvetlenül nem értelmezhető, szükséges volt egy olyan adatkiértékelő rendszerre, amely képes a kémiai információt szövettani jellegű információvá lefordítani. Ehhez a "fordításhoz" természetesen szükség van egy "szótárra", azaz egy olyan adatbázisra, amely ismert szövetek tömegspektrumait tartalmazza. Ennek az adatbázisnak az alapjait, valamint a fordító algoritmust sikeresen létrehoztuk. A jelenlegi kísérleti rendszerünk képes a tömegspektrometriás elemzést, valamint az adatfeldolgozást egy másodpercen belül végrehajtani, azaz egy másodpercen belül visszajelezni a sebésznek, hogy éppen milyen szövettípust vág az eszköz.
A készülék elképzeléseink szerint alapvetően kétféleképpen használható: egyrészt normális sebészeti beavatkozás során képes figyelmeztető jelzést adni a sebésznek, ha túlságosan megközelíti a rákos daganatot, valamint az eszköz használható célzott azonosításra is, a sebészeti területen látható, gyanús szövetrészletek esetében
A kutatás jelenlegi állása
Az eddigi fejlesztések során létrehoztunk egy, humán sebészeti környezetben üzemeltethető eszközt, amelyet először állatorvosi környezetben, majd később tényleges sebészeti környezetben teszteltünk.
A Kutatóegyetemi címnek köszönhetően jelenleg két, identikus készülék üzemel műtőkben. Bár ezeket a készülékeket napi szinten használják, a használat egyelőre csak a mintavételre, azaz a fentebb említett adatbázis bővítésére szorítkozik. Az adatbázis reményeink szerint ez év második felére éri el azt a méretet, hogy megkezdhessük a készülék engedélyeztetését, és tényleges diagnosztikai felhasználását.
Eközben folyik a készülék funkcionális tesztelése is, állatorvosi környezetben. Állatorvosi praxisból szármzó rákos kutyákat műtünk az eszköz segítségével, és összehasonlítjuk a műtétek hatékonyságát a hagyományos módon történő műtétekével, amely vizsgálatok úgyszintén elengedhetetlenek a sikeres engedélyeztetéshez.
Oncompass Medicine Precíziós Onkológiai Program
Az Oncompass Medicine molekuláris diagnosztikai laboratóriuma és információs központja a molekuláris diagnosztika legfrissebb eredményeit és módszereit alkalmazva igyekszik megtalálni a daganatos betegségben szenvedők számára az adott időpontban legmegfelelőbb kezelési lehetőségeket.
Miben tudunk segíteni?
A Precíziós Onkológiai Programunkban a személyre szabott onkológiai ellátás lehetőségeit mutatjuk be a daganatos betegek számára.
Minden daganatos megbetegedés genetikai eredetű, és számos, a daganatot okozó génhiba esetében már személyre szabott onkológiai kezelés adható. A molekuláris diagnosztika a daganatos betegség okát tárja fel, az azonosított génhibák alapján egy speciális onkológiai szoftver segítségével meghatározzuk a daganat támadáspontját (molekuláris célpont) és a célponttal összefüggésbe hozható személyre szabott gyógyszereket. A személyre szabott onkológiai ellátáshoz több feltételnek kell megfelelnie, ennek felméréséhez kérjen időpontot személyes konzultációra!
A személyre szabott kezelési terv minden olyan daganattípusban felállítható, amelyben az azonosított génhibáknak megfelelő kezelés elérhető.
Virtuális Molekuláris Tumor Board
A VMTB szolgáltatás keretében az Oncompass Medicine egyedülálló módon kezelőorvosok és onkoteamek számára biztosít szakmai támogatást annak érdekében, hogy betegeiknek a nemzetközi ajánlásoknak megfelelő, legkorszerűbb precíziós onkológiai ellátást nyújthassák.
Az Oncompass Precíziós Onkológiai Program keretében igénybe vehető szolgáltatás során rugalmasan igazodunk a klinikusi igényekhez, a hét bármely napján, különböző időpontokban biztosítunk lehetőséget az esetek megbeszélésére, amely az adatvédelmi előírásoknak megfelelően, biztonságos online platformon történik.
(hirdetés)
Tisztelt Olvasónk! Felhívjuk a figyelmét, hogy anyagaink tájékoztató és ismeretterjesztő jellegűek, így nem adhatnak választ minden olyan kérdésre, amely egy adott betegséggel vagy más témával kapcsolatban felmerülhet, és főképp nem pótolhatják az orvosokkal, gyógyszerészekkel vagy más egészségügyi szakemberekkel való személyes találkozást, beszélgetést és gondos kivizsgálást.